Estrategia de vacunación en México y diversidad de vacunas.
La estrategia de vacunación anti-COVID-19 ha generado mucha polémica a nivel mundial, y en específico, en México. Las fuentes de dichas polémicas probablemente se relacionen a un entendimiento pobre en cuanto a la diversidad de vacunas y sus características, las distintas condiciones de almacenamiento y transporte que requieren las diversas formulaciones, y otros aspectos estratégicos relativos a la priorización de la población a vacunar. En este artículo intentaremos explicar dichas polémicas.
La vacunación anti-COVID-19 es una prioridad nacional, y la planeación de su distribución es compleja.
Las vacunas tienen distintos grados de eficacia, sin embargo, todas son buenas opciones en la regulación de los rubros más importantes.
Es necesario un replanteamiento de la priorización de vacunación
SARS-CoV-2
COVID-19
Vacunación
Prevención primaria
- Introducción
Según la Organización Mundial de la Salud (OMS) se reportaron los primeros casos de COVID-19, infección derivada del virus SARS-CoV-2, en Wuhan, China a principios de diciembre de 2019. Investigaciones sugieren que el virus tiene un origen natural debido a sus características genómicas, pues carece de mezclas de elementos conocidos. Debido a que tanto el virus SARS-CoV-1 y SARS-CoV-2 están estrechamente relacionados con otros coronavirus aislados de murciélagos se sugiere que tuvieron su origen en poblaciones de murciélagos1, aunque también se hipotetiza que el origen del virus podría haber ocurrido en el pangolín2, pero muchos datos adicionales son necesarios para clarificar su origen.
Según el último reporte (21/04/21) a nivel mundial, desde los orígenes de la pandemia se acumulan más de 143 millones de casos por COVID-19, 62 millones de personas recuperadas y 3 millones de muertes3. Dicha entidad también ha generado pérdidas económicas del 5.6% del producto interno bruto a nivel mundial4.
Aunque la investigación al respecto de un tratamiento está considerablemente avanzada considerando el corto tiempo que ha transcurrido desde el advenimiento de la enfermedad, las guías de práctica clínica de COVID-19 recomiendan únicamente el uso de corticoesteroides (principalmente dexametasona), tocilizumab y el remdesivir5. No obstante, exceptuando a los primeros, los medicamentos recomendados tienen un costo muy alto y una disponibilidad muy pobre. Así mismo, la terapia con anticuerpos monoclonales o plasma convaleciente se encuentra en constante evaluación, pero no se ha emitido una recomendación frente a su uso5. Sin embargo, aun contando con la aprobación de las instancias correspondientes, ambos tipos de terapia serán costosas y de disponibilidad limitada.
En estas circunstancias, la vacunación es reconocida como una estrategia más óptima para la mitigación de la pandemia, pues el costo por dosis es muy bajo, y la prevención de los casos graves de la enfermedad así como la inmunidad esterilizante podrían evitar la hospitalización y muerte de los pacientes afectados, así como la propagación de la enfermedad, junto con las repercusiones económicas que esto acarrea6.
Según un informe de la OMS, actualmente varios países han desarrollado una gran diversidad de vacunas contra el virus SARS-CoV-2, sumando hasta 91 opciones en desarrollo clínico y 184 en una fase preclínica de desarrollo. De estas, algunas han probado su eficacia, destacando las de Pfizer-BioNTech, AstraZeneca-Oxford, Sputnik V (Gamaleya Research Institute), CVnCoV (Curevac), CoronaVac (Sinovac), Moderna Inc. y CanSino Bio7. Incluso, algunos países ya iniciaron con la vacunación contra la COVID-19 son Reino Unido, Estados Unidos, Rusia, Puerto Rico, Costa Rica, Chile y México; con Estados Unidos y Chile liderando la aplicación de vacunas en el continente americano, Reino Unido en Europa e Israel en Oriente8.
- Estrategia de vacunación en México.
En México la vacunación anti-SARS-CoV-2 inició el 24 de Diciembre del 2020, cuatro meses después, con una aplicación promedio 0.3 dosis por cada 100 habitantes, se ha logrado inocular a 8.3% de la población, lo que equivale a 14.37 millones de dosis aplicadas8. Este logro se ha desprendido de un esfuerzo titánico, así como de una profunda planeación.
Parte importante de dicha estrategia es la distribución de la vacuna considerando sus propiedades de almacenamiento y las características de las regiones en donde será aplicada: en zonas rulares es mejor el uso de vacunas que requieren congelación y/o refrigeración, ya que la falta de redes de transporte en ultracongelación en este tipo de zonas no existen, pero sí son comunes las primeras mencionadas. En cambio, para zonas urbanas es mejor el uso de vacunas que requieran ultracongelación, debido al mayor acceso a tecnología de ultracongelación adecuada9.
Esto es derivado de que la primera vacuna que se encontró ampliamente disponible para México (Pfizer-BioNTech) y el mundo se desarrolló en una plataforma de ARN mensajero, la cual cuenta con requerimientos exquisitos de transporte en red fría. Se debe almacenar a -70°C y consta de una vida útil de 5 días en un rango de temperaturas que varía entre los 2°C a los 8°C. Una vez reconstituida su vida útil se reduce a 6 horas9.
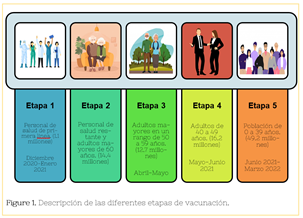
La estrategia de mitigación contra el virus SARS-CoV-2 propuesta consta de cinco etapas para la distribución de vacunas y refuerzos a la población mexicana9 (Fig. 1):
En la primera etapa (diciembre 2020- enero 2021) la vacuna se entregó al personal de salud de primera línea del control de COVID-19. Se estima una cantidad de 1.1 millones de personas.
La segunda etapa (febrero-abril 2021) consta de la aplicación de la vacuna al personal de salud restante, y a adultos mayores de 60 años o más. Estimando así la vacunación de 14.4 millones de personas.
En la tercer etapa (abril-mayo 2021) se consideran a las personas de entre 50 a 59 años de edad, las cuales se estima que sean 12.7 millones.
La cuarta etapa (mayo-junio 2021) empieza la aplicación a personas de 40 a 49 años, la población se estima que consta de 16.2 millones.
Por último la quinta etapa (junio 2021- marzo 2022) el resto de la población que consta de 49.2 millones de personas.
La Ciudad de México, Coahuila, Estado de México, Querétaro y Nuevo León dieron inicio a la primera etapa funcionando como lugares de calibración de la estrategia, mientras que el día 12 de enero de 2021 se comenzó a distribuir al resto del país9. En adición se propuso implementar una estrategia llamada Operativo correcaminos, la cual consiste en lograr distribuir eficazmente la vacuna a la población susceptible en zonas rurales, posteriormente a aquellos que residan pequeñas y medianas ciudades, por último a aquellos que residan en áreas metropolitanas para completar la etapa 2 de manera eficaz9.
De acuerdo con las estimaciones del gobierno mexicano las etapas 3,4 y 5 contarán con mayor variedad de vacunas según la disponibilidad de las mismas, así como la autorización de la COFEPRIS. Las vacunas CanSino y AstraZeneca tendrán una logística diferente y con mayor afinidad al programa de vacunación universal debido a sus características de refrigeración convencionales es decir de entre 2 a 8°C9, por lo que destacará su uso en estas etapas.
La vigilancia de la introducción de nuevas vacunas así como su seguimiento estarán a cargo del sistema de vigilancia Eventos Supuestamente Atribuidos a la Vacunación o Inmunización (ESAVI). Garantizando la identificación y monitorización de aquellos eventos que estén relacionados con la aplicación de las vacunas, el proceso de administración o sus componentes. Se llevará a cabo en unidades del sector salud dónde se pueden identificar por un usuario, su familia o el resto del personal, y se monitorea en los 30 días posteriores9. De esta forma, se plateó en los próximos 15 meses inmunizar al 70% del país, lo suficiente para alcanzar la inmunidad de rebaño para un patógeno similar al SARS-CoV-2.
En México existen actualmente cuatro convenios para la procuración de vacunas a la población mexicana9, los cuales son los siguientes:
- Convenio COVAX
COVAX es una organización filantrópica que acelera el acceso a una amplia cartera de vacunas en países de bajos ingresos, donde financia la vacunación de al menos el 20% de su población.
- Convenio AstraZeneca
El primero de enero de 2021, México otorgó la autorización de emergencia para la vacuna contra COVID-19 desarrollada por el laboratorio AstraZeneca y la Universidad de Oxford. El convenio consiste en que México en acuerdo con la fundación del magnate mexicano Carlos Slim, AstraZeneca y la Universidad de Oxford autoriza la producción del biológico en su territorio y Argentina así como su distribución sin fines de lucro en América Latina, excepto Brasil, facilitando la compra de hasta 200 millones de dosis, permitiendo así inmunizar gratuitamente.
- Convenio CanSino
La empresa CanSino, lleva a cabo en nuestro país un estudio clínico fase III, se firmó un contrato para la adquisición de 35 millones de dosis para vacunar a la población mexicana, de igual forma será envasada dentro del territorio por los laboratorios Drugmex.
- Convenio Pfizer
Se firmó un contrato para la fabricación y adquisición de 34.4 millones de dosis, se espera que para marzo se haya alcanzado la entrega de cinco millones 181 mil 150 dosis a nuestro país. Dicha vacuna será universal, gratuita y de fácil acceso para la población.
- ¿Podría ser mejor la distribución de vacunas?
La estrategia del operativo correcaminos se ha basado en la observación de que las personas con edad >55 años tienen un riesgo más elevado de morir a causa de COVID-19 que las personas menores10 a dicha edad, por lo que se les ha dado prioridad a los adultos mayores en la estrategia de vacunación. No obstante, se han hecho críticas a este sistema fundamentadas en la idea de que las personas mayores tienen una probabilidad incrementada de morir por causas no relacionadas a COVID-19 con respecto a la población más joven.
En nuestra opinión esto no reduce la importancia que tiene el darle la oportunidad de cuidarse adecuadamente a las personas, sin embargo creemos que la priorización en la vacunación podría ser mejor de acuerdo con otro tipo de datos.
En primer lugar, miembros de nuestro equipo han participado en estudios de cohorte internacionales donde se ha determinado que los pacientes que son sometidos a cirugías de cualquier especialidad después de haber padecido COVID-19 tienen un incremento en la mortalidad del 23.8%, mientras que las complicaciones pulmonares ocurren en el 38% de ellos11. Siguiendo la misma línea de pensamiento, estudiamos a continuación cuánto tiempo debía pasar después de padecer COVID-19 para que la cirugía no implicase un riesgo adicional de mortalidad, encontrando que el tiempo óptimo para realizar las intervenciones es de siete semanas12. En muchas ocasiones, sin embargo, no puede pasar tanto tiempo para que el paciente se someta a cirugía, por ejemplo en cesáreas, remoción de tumores, ciertas colecistectomías, etc. En estas circunstancias, entonces, se vuelve mandatorio realizar otro tipo de intervención. Así, un último estudio en el que participamos, donde se tomaron en cuenta los datos de probabilidad de muerte según el sector etario y el tipo de cirugía, demuestran que si se diera prioridad en los programas de vacunación a la gente que será sometida a cirugía electiva, en lugar de a la población general, se podrían salvar 58, 657 vidas en un año13. De esta forma, la priorización de sectores poblacionales podría ser optimizada tomando en cuenta estos datos, que se obtuvieron de 140,231 pacientes pertenecientes a 116 países.
Sin embargo, otra propuesta interesante es la de priorizar la vacunación del sector económicamente activo. En términos generales se ha observado que el sector etario donde existen más contagios está entre 20-59 años, que representa el sector económicamente activo14. Creemos que si se vacunase primero a dicho sector, la cantidad de contagios disminuiría considerablemente, reduciendo la incidencia general de la enfermedad, y repercutiendo en los adultos mayores que reciben cuidados por parte de los adultos en edad productiva. En este tenor, una estrategia potencialmente eficiente, sería el de vacunar en un principio a los trabajadores de los sectores laborales más esenciales, que son el energético, el hospitalario y el alimenticio. Esta idea se desprende del hecho de que estos sectores nunca frenaron sus labores, a modo de que no colapsara la sociedad, y por lo mismo se han expuesto más a los contagios. Posteriormente, podría ser una buena idea vacunar a los trabajadores de los siguientes sectores laborales, según la urgencia de sus actividades.
- Alternativas de vacunación
Debido a estos convenios, la diversidad de vacunas anti-COVID-19 disponibles en México es grande, y tiene altas probabilidades de ser aún más grande. En estas circunstancias, muchas preguntas acerca de las distintas vacunas pueden ser planteadas: ¿qué vacuna es mejor?, ¿existen vacunas malas?, ¿qué tan seguras son?, ¿los estudios acerca de su seguridad son pertinentes?
A manera de aclarar estas y otras preguntas, en la Tabla 1 se resumen las principales características de las vacunas que se aplican en México, o que tienen una alta probabilidad de ser aplicadas en un futuro cercano.
Tabla 1. Principales vacunas anti-COVID-19 y sus características.
| Fabricante | Vacuna | Tipo de vacuna | Dosis/espacio | Eficacia para prevenir COVID-19 sintomático | Eficacia para combatir COVID-19 severo | Voluntarios en los estudios | Referencia |
| Pfizer-BioNTech | BNT162b2 | mRNA | 2/21 días | 52% 1D 94.6% 2D | 95-100% | 43,880 | 15 |
| Moderna Incorporated | mRNA 1273 | mRNA | 2/28 días | 92.1% 1D 94.1% 2D | 100% | 30,420 | 16 |
| Johnson & Johnson | Ad26.COV2.S | Vector viral | 1 | 66% | 76.7% | 39,321 | 17 |
| AztraZeneca-Oxford | ChAdOx1 (AZD1222) | Vector viral | 2/28 días | 64.1% 1D 70.4% 2D | 100% | 23,848 | 18 |
| Novavax Inc. | NVX-Cov2373 | Subunitaria | 2/30 días | 89.3% 2D | 98.3% | 37,000 | 19 |
| CureVac-GlaxoSmithKline | CVnCoV | mRNA | 2/21 días | Seroconversión en 52-75% | Desconocido | 880 | 20 |
| Gamaleya National Research Center | Gam-COVID-Vac (Sputnik V) | Vector viral | 2/21 días | 87.6% 1D 91.6% 2D | 100% | 41,843 | 21 |
| Sinovac Biotech | Coronavac | Virus inactivado | 2/14 días | 51-84%, Seroconversión en 97% | 85-100% | 1,309 | 22-24 |
| Sinopharm | BBIBP-CorV | Virus inactivado | 2/21 días | 78.1% | 78.7% | 16,671 | 25 |
| CanSino Biologicals/Beijing Institute of Biotechnology | Ad5-nCoV | Vector viral | 1 | 68.83% | 95.47% | 1,211 | 26,27 |
| Janssen Pharmaceutical | Ad26.COV2.s | Vector viral | 2/56 días | 66.9% | 85.4% | 39,050 | 28 |
Es importante destacar que en todos los estudios iniciales que se realizan para medir la eficacia de una vacuna existen tres desenlaces a estudiar: la primera es la capacidad de las vacunas para reducir la probabilidad de desarrollar una infección sintomática, que es, en la opinión pública, el rasgo más importante a evaluar. Y si bien es importante abatir las manifestaciones clínicas de la enfermedad, es más útil el siguiente rasgo, que es el abatimiento de las presentaciones severas de la enfermedad. En el imaginario colectivo la primera opción es lo que determina la eficacia de una vacuna, llegando a criticar a aquellas opciones que no superan el 90% de eficacia, no obstante, una infección sintomática leve podría manifestarse de forma tan simple como un resfriado común. En cambio, las infecciones severas son tan fuertes que hacen peligrar la vida. De esta forma, todas las opciones de vacunación anti-COVID-19 son altamente eficientes en la modulación del parámetro que tiene mayor trascendencia.
El último parámetro que se evalúa en estos estudios es la seguridad. Y este parámetro le preocupa a mucha gente, pues se tiene la idea de que se han hecho de forma muy precipitada. Sin embargo, los estudios de seguridad que se han hecho para las vacunas anti-COVID-19 son los más exhaustivos e intensivos que se han hecho en la historia de las vacunas. Una razón para este argumento es que usualmente los estudios de seguridad de un determinado fármaco se realizan dando seguimiento a 1,000-3,000 pacientes29, mientras que el tamaño de los estudios que se han hecho para las vacunas anti-COVID-19 llega a ser hasta 10 veces mayor (Tabla 1).
Más aún, en los estudios de seguridad de otros fármacos se da un seguimiento limitado a la duración del mismo estudio, por lo que una vez que estos concluyen, se dejan de estudiar las repercusiones que los medicamentos pudiesen tener para el resto de la población en la que se administra. No obstante, para darle un mayor grado de seguimiento a las vacunas anti-COVID-19 se creó en estados unidos un programa de monitoreo llamado “vaccine adverse event reporting system”, o por sus siglas en inglés, VAERS30. Dicho sistema ha dado seguimiento a más de 245 millones de dosis aplicadas hasta el momento, reportando sólo 4,178 muertes (0.0017%), de las cuales ninguna demostró estar asociada a la vacunación de forma directa, después de una investigación exhaustiva.
- Conclusiones
La vacunación anti-COVID-19 podría ser la única manera de terminar efectivamente con la pandemia por el patógeno SARS-CoV-2. Aun cuando existen preocupaciones por parte del público general acerca de la seguridad y eficacia de las vacunas, todas son buenas opciones en cuanto a la prevención de formas severas de la enfermedad, que es el parámetro más importante en cuanto a su utilidad. Por otra parte, los estudios acerca de su seguridad son los mejores que se han hecho en la historia de la medicina, y el seguimiento ha trascendido la duración de los estudios. Así, creemos que la vacunación anti-COVID-19 puede ser recomendada a un público amplio.
Si bien en México el acceso a la vacunación ha sido lento para los sectores etarios menores, y la distribución de las “mejores” vacunas ha sido desigual, el compromiso de vacunar a todos los mexicanos se está cumpliendo y a todos se les ha vacunado con biológicos de elevada calidad, aprovechando las mejores cualidades de cada tipo de vacuna conforme a la red fría de cada localidad. La única crítica sólida que podría plantearse es que la estrategia de distribución de vacunas pudiese ser mejor, protegiendo primero a los sectores que están en mayor riesgo de contagio o mortalidad, por ejemplo a personas económicamente activas y/o que serán sujetas a una cirugía electiva. Sin embargo, cada vez se está más cerca de la solución, y sólo es momento de esperar nuestro turo para vacunaros tomando una decisión responsable y basada en datos.
- Agradecimientos
Los autores desean agradecer a la Sociedad Española de Beneficencia por poner al alcance del público esta información de manera gratuita.
- Declaración de conflictos de interés
Ninguno de los autores tiene conflictos de interés que declarar.
- Referencias
1 Salud, O. M. d. l. COVID-19 timeline, <https://www.who.int/es/news/item/29-06-2020-covidtimeline> (2020).
2 Zhang, T., Wu, Q. & Zhang, Z. Probable Pangolin Origin of SARS-CoV-2 Associated with the COVID-19 Outbreak. Current biology : CB 30, 1346-1351.e1342, doi:10.1016/j.cub.2020.03.022 (2020).
3 University, J. H. COVID-19 Dashboard by the Center for Systems Science and Engineering (CSSE), <https://www.arcgis.com/apps/opsdashboard/index.html#/bda7594740fd40299423467b48e9ecf6> (2020).
4 Statista. Impact of the coronavirus pandemic on the global economy - Statistics & Facts, <https://www.statista.com/topics/6139/covid-19-impact-on-the-global-economy/> (2021).
5 Health, N. I. o. COVID-19 Treatment Guidelines, <https://www.covid19treatmentguidelines.nih.gov/whats-new/> (2021).
6 Durán-Méndez, A., Jardínez-Vera, A. C., Jiménez-Muñoz, E. & Peón, A. N. A brief history of vaccines and an overview of their benefits. Revista de la Sociedad Española de Beneficencia 2, 6, doi:https://doi.org/10.46295/2:1.VACHI (2021).
7 Organization, W. H. Draft landscape and tracker of COVID-19 candidate vaccines, <https://www.who.int/publications/m/item/draft-landscape-of-covid-19-candidate-vaccines> (2021).
8 Ritchie, H. et al. Coronavirus (COVID-19) Vaccinations, <https://ourworldindata.org/covid-vaccinations> (2021).
9 Cortés Alcalá, R., Gómez Torres, R. & Alba Ricaño, X. (ed Dirección General de Promoción de la Salud) 1-39 (Gobierno de México, 2021).
10 Gallo Marin, B. et al. Predictors of COVID-19 severity: A literature review. Reviews in medical virology 31, 1-10, doi:10.1002/rmv.2146 (2021).
11 Collaborative, C. O. Mortality and pulmonary complications in patients undergoing surgery with perioperative SARS-CoV-2 infection: an international cohort study. Lancet 396, 27-38, doi:10.1016/S0140-6736(20)31182-X (2020).
12 Collaborative, C. O. & GlobalSurg, C. Timing of surgery following SARS-CoV-2 infection: an international prospective cohort study. Anaesthesia76, 748-758, doi:10.1111/anae.15458 (2021).
13 Covidsurg Collaborative, G. C. SARS-CoV-2 vaccination modelling for safe surgery to save lives: data from an international prospective cohort study. The British journal of surgery, doi:10.1093/bjs/znab101 (2021).
14 Department of Health, A. G. COVID-19 cases by age group and sex, <https://www.health.gov.au/resources/covid-19-cases-by-age-group-and-sex> (2021).
15 Polack, F. P. et al. Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine. The New England journal of medicine 383, 2603-2615, doi:10.1056/NEJMoa2034577 (2020).
16 Walsh, E. E. et al. Safety and Immunogenicity of Two RNA-Based Covid-19 Vaccine Candidates. The New England journal of medicine 383, 2439-2450, doi:10.1056/NEJMoa2027906 (2020).
17 Sadoff, J. et al. Safety and Efficacy of Single-Dose Ad26.COV2.S Vaccine against Covid-19. The New England journal of medicine, doi:10.1056/NEJMoa2101544 (2021).
18 Voysey, M. et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet 397, 99-111, doi:10.1016/s0140-6736(20)32661-1 (2021).
19 Shinde, V. et al. Efficacy of NVX-CoV2373 Covid-19 Vaccine against the B.1.351 Variant. The New England journal of medicine, doi:10.1056/NEJMoa2103055 (2021).
20 Goepfert, P. A. et al. Safety and immunogenicity of SARS-CoV-2 recombinant protein vaccine formulations in healthy adults: interim results of a randomised, placebo-controlled, phase 1-2, dose-ranging study. The Lancet. Infectious diseases, doi:10.1016/S1473-3099(21)00147-X (2021).
21 Logunov, D. Y. et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. Lancet 397, 671-681, doi:10.1016/S0140-6736(21)00234-8 (2021).
22 Wu, Z. et al. Safety, tolerability, and immunogenicity of an inactivated SARS-CoV-2 vaccine (CoronaVac) in healthy adults aged 60 years and older: a randomised, double-blind, placebo-controlled, phase 1/2 clinical trial. The Lancet. Infectious diseases, doi:10.1016/s1473-3099(20)30987-7 (2021).
23 Zhang, Y. et al. Safety, tolerability, and immunogenicity of an inactivated SARS-CoV-2 vaccine in healthy adults aged 18-59 years: a randomised, double-blind, placebo-controlled, phase 1/2 clinical trial. The Lancet. Infectious diseases21, 181-192, doi:10.1016/S1473-3099(20)30843-4 (2021).
24 (SAGE), S. A. G. O. E. Evidence Assessment: Sinovac/CoronaVac COVID-19 vaccine. (World Health Organization, 2021).
25 (SAGE), S. A. G. O. E. (ed World Health Organization) 16 (2021).
26 Zhu, F. C. et al. Safety, tolerability, and immunogenicity of a recombinant adenovirus type-5 vectored COVID-19 vaccine: a dose-escalation, open-label, non-randomised, first-in-human trial. Lancet 395, 1845-1854, doi:10.1016/S0140-6736(20)31208-3 (2020).
27 Díaz Ortega, J. L. Vol. 2021 (ed Programa de Atención a la Salud de la Infancia y la Adolescencia. Centro Nacional para la Salud de la Infancia y la Adolescencia) 25 (Gobierno de México, 2021).
28 Vaccines and Related Biological Products Advisory Committee Meeting, F. 62 (2021).
29 Research, C. Phases of clinical trials, <https://clinicalresearchs.info/phases-of-clinical-trials/> (2020).
30 Services, D. o. H. a. H. Vaccine Adverse Events Reporting System (VAERS), <https://vaers.hhs.gov/> (2020).
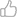 0
0
 0
0